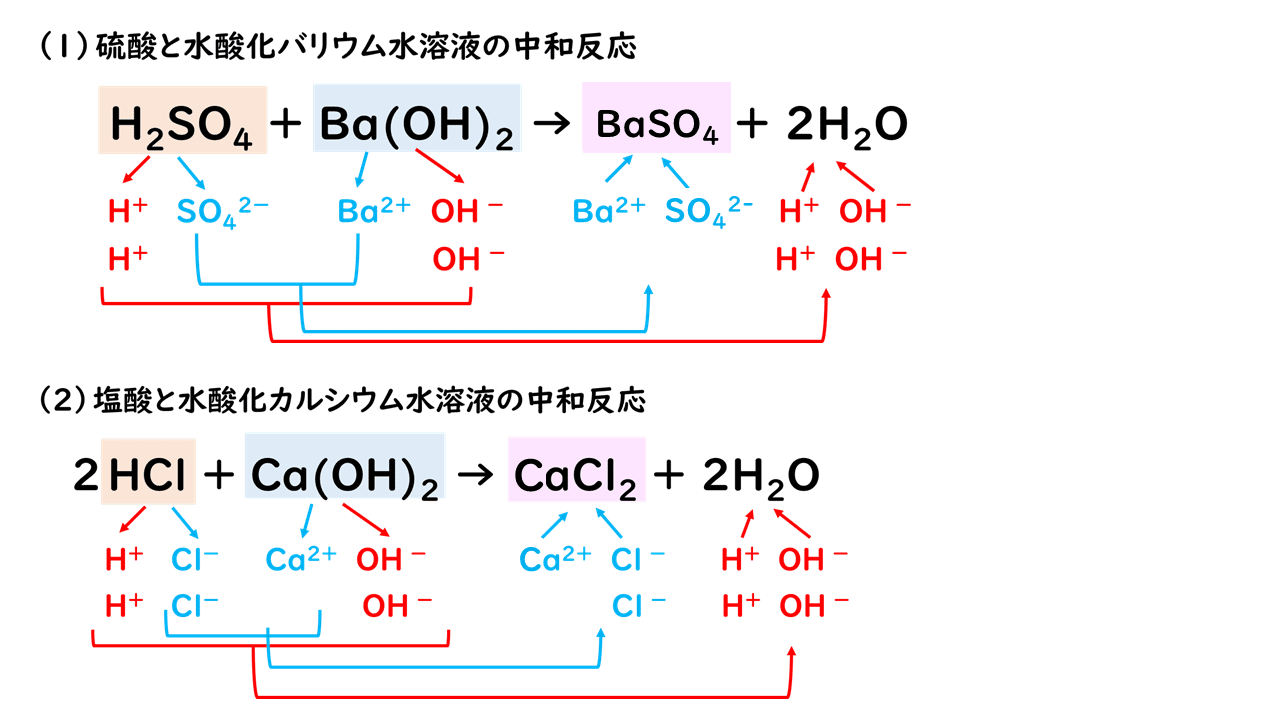
中3化学 中和反応 中学理科 ポイントまとめと整理
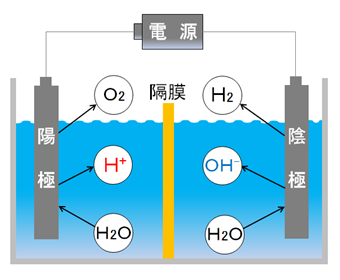
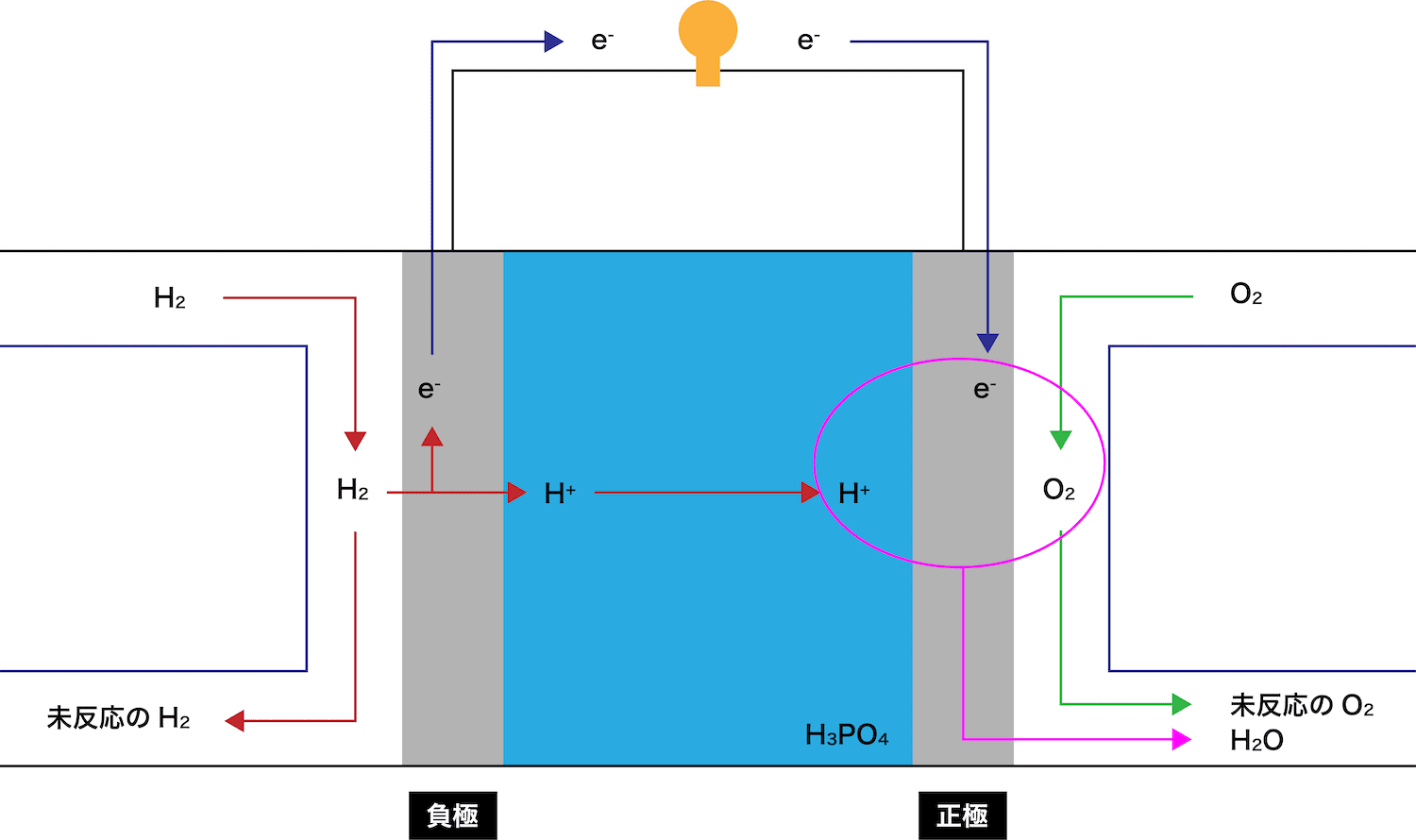
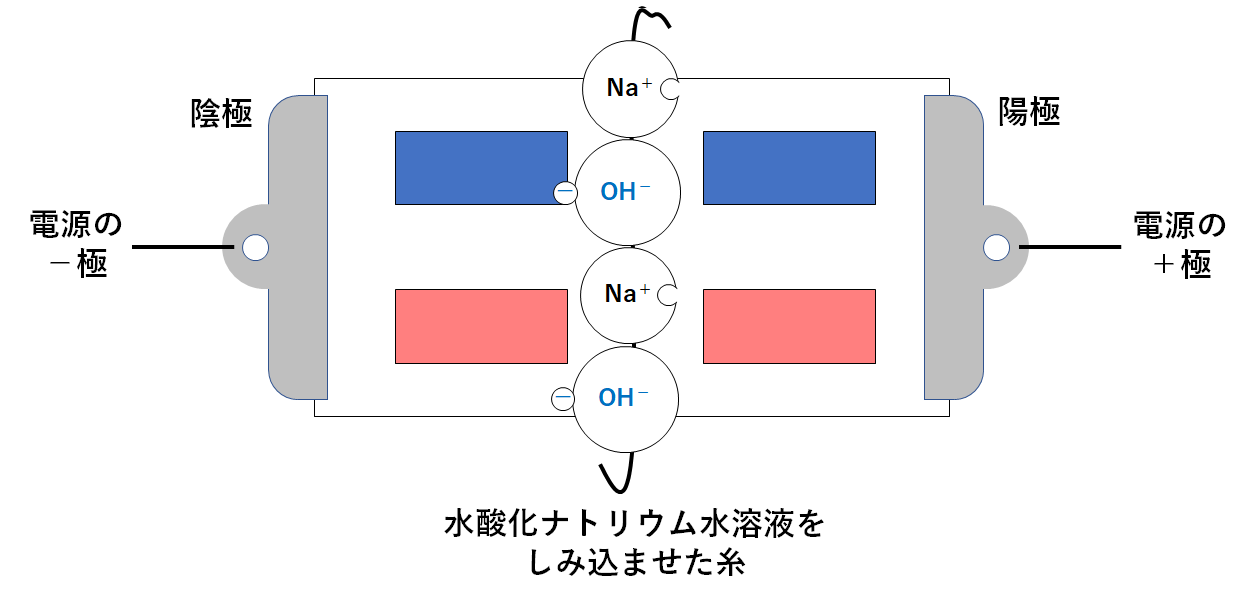
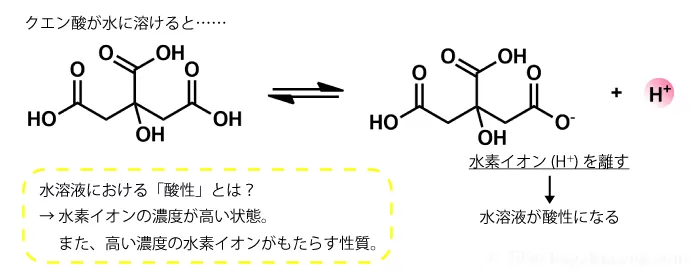
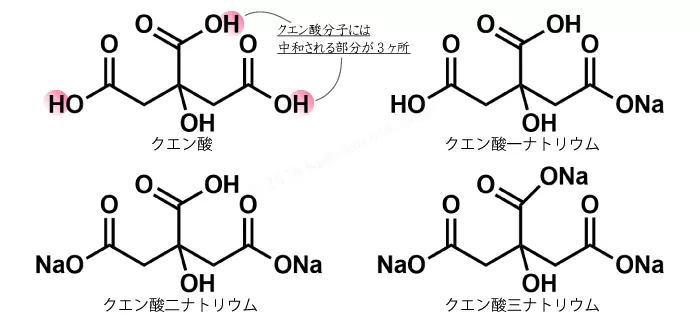
分子式 c 6 h 8 o 7 は、クエン酸分子を構成する 原子の種類と数のみ を示し、分子構造や性質は伝えられない化学式です。 構造式 は分子構造、すなわち、 原子の繋がり方を示す 化学水素製造の反応は外部から電源を電極へ図1のように加え、陰極側へ水溶液を供給すると、水電解の反応は(1)、(2)式のように、 陰極に供給された水(2h 2 o)と外部電源からやって来る電
アルカリ性 水溶液 化学式
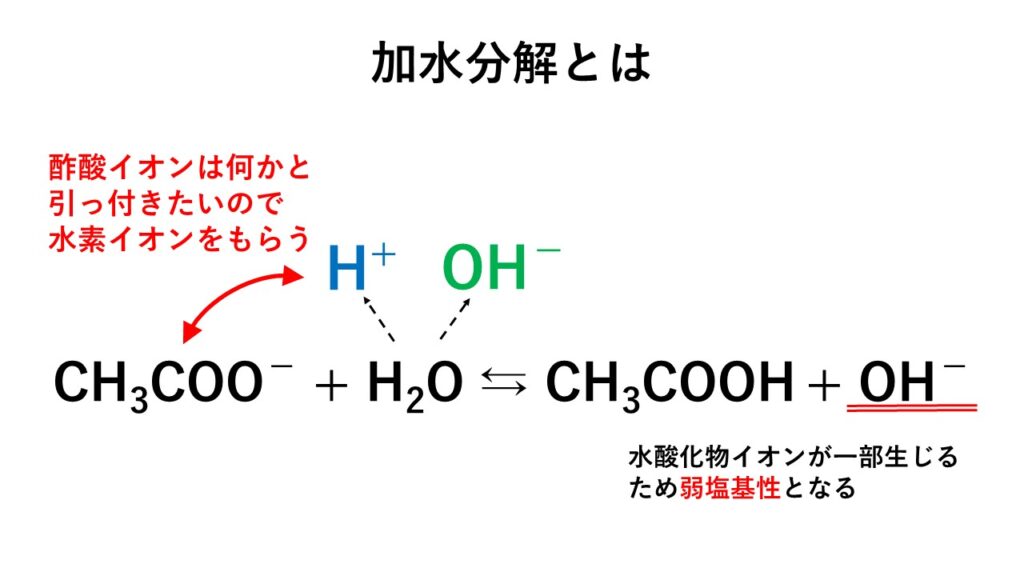
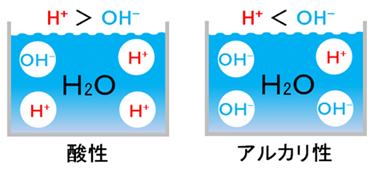
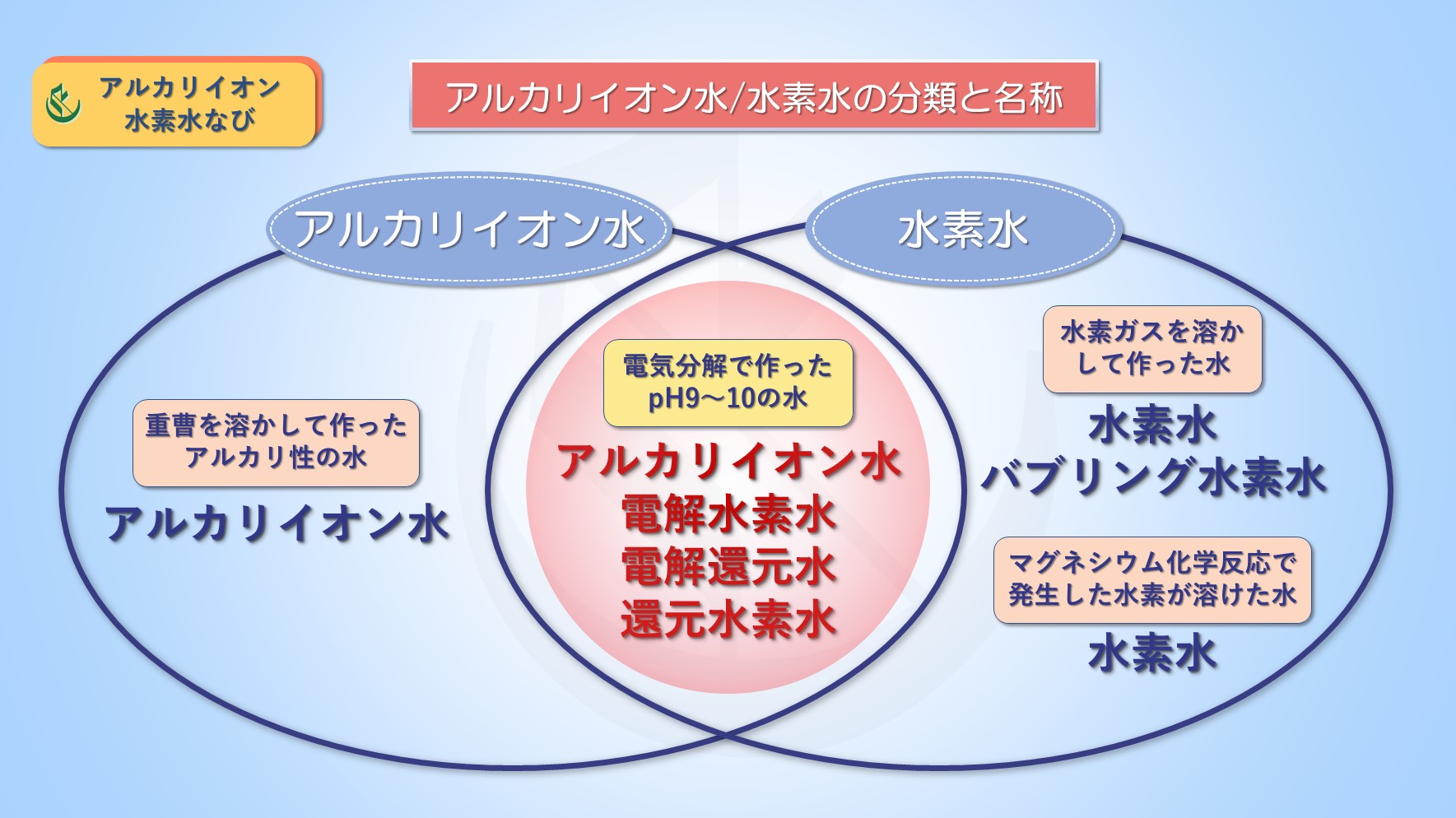
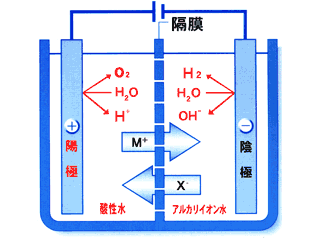
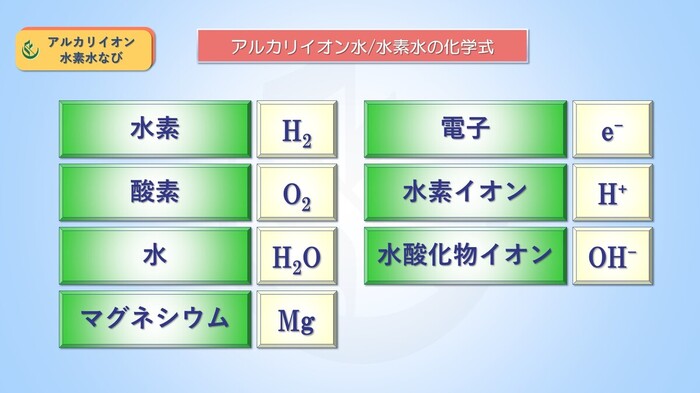
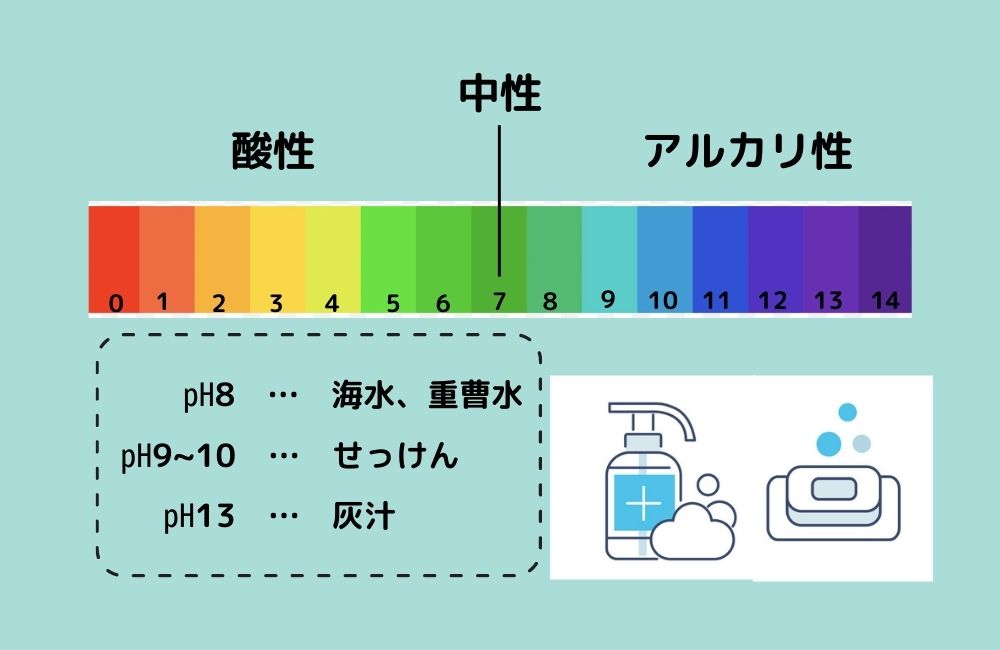
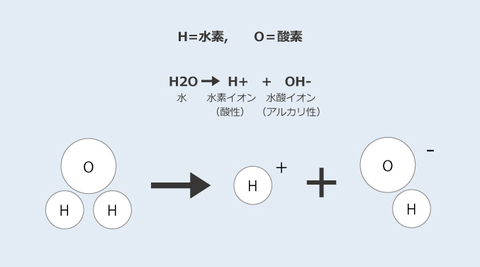
アルカリ性 水溶液 化学式- ・アルカリは水溶液中で ー O H ー (水酸化物イオン)を放出するもの です。 アルカリは水酸化物イオンを出すことで酸の働きを打ち消すことができます。 + H + (水素イオン)とここでは説明のために、 飲用可能なものをアルカリイオン水(pH9〜10) 、 飲用不適のものをアルカリ性電解水(pH10〜) と分けるが、本来はそういった区別はない。 成分は水酸化ナトリウム、

6 1 酸と塩基 おのれー Note
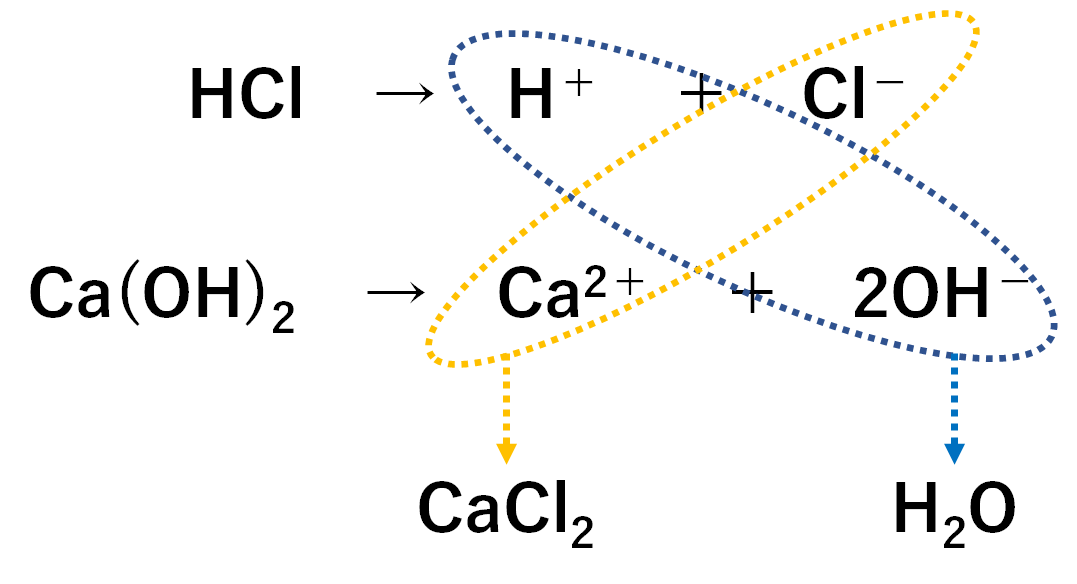
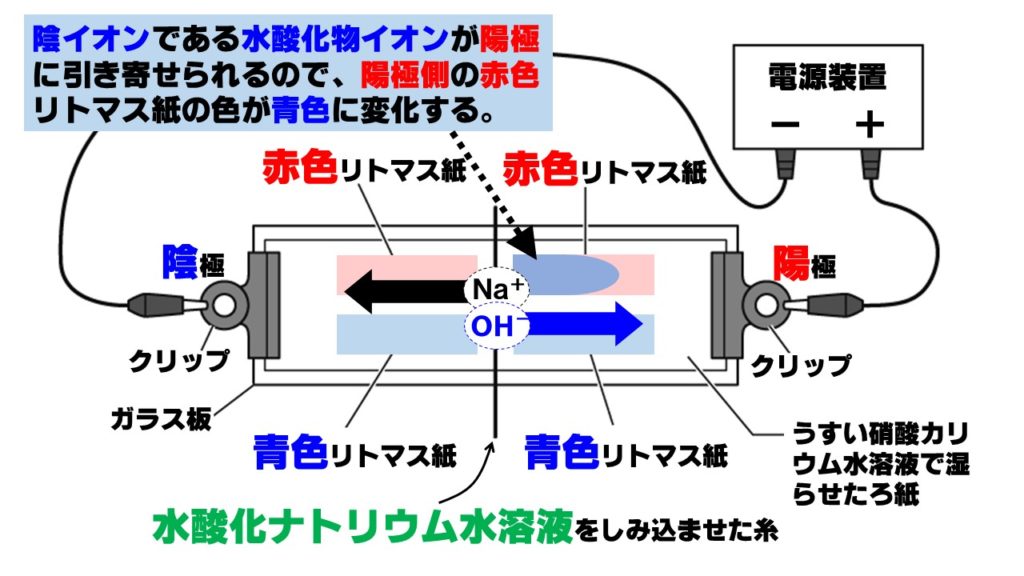
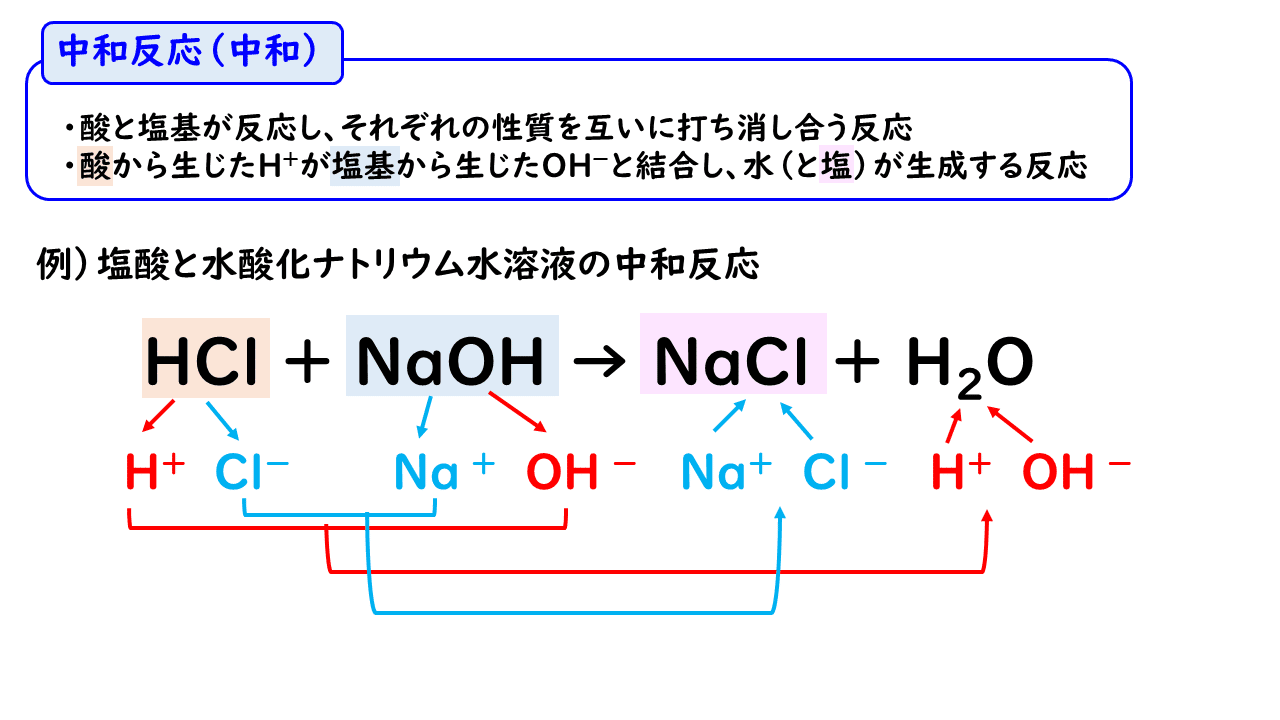
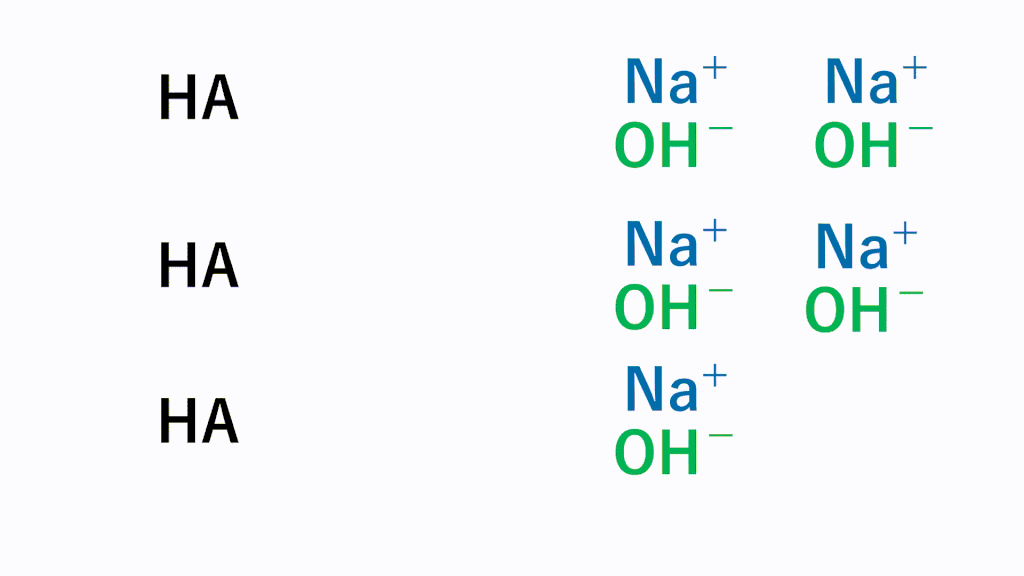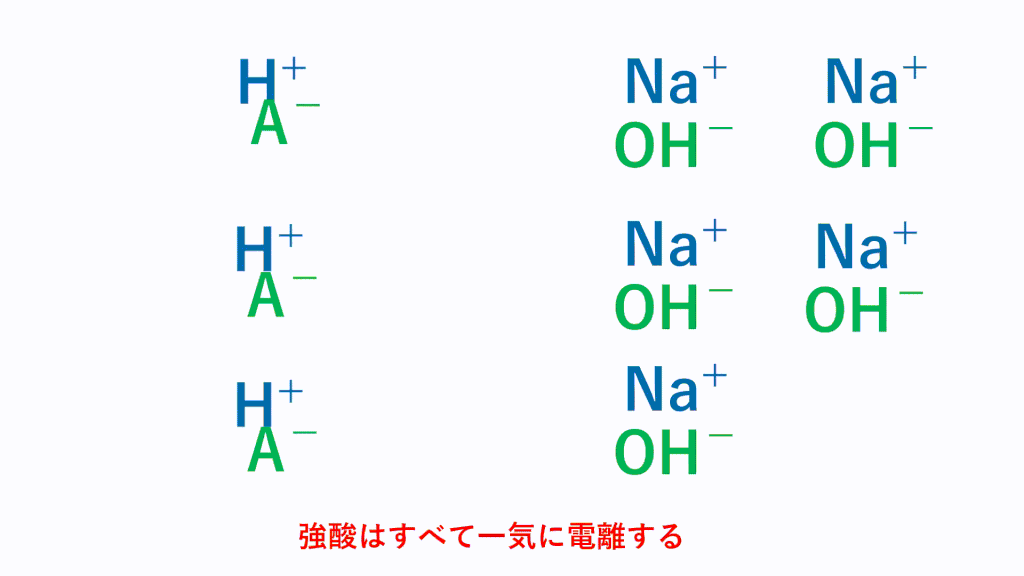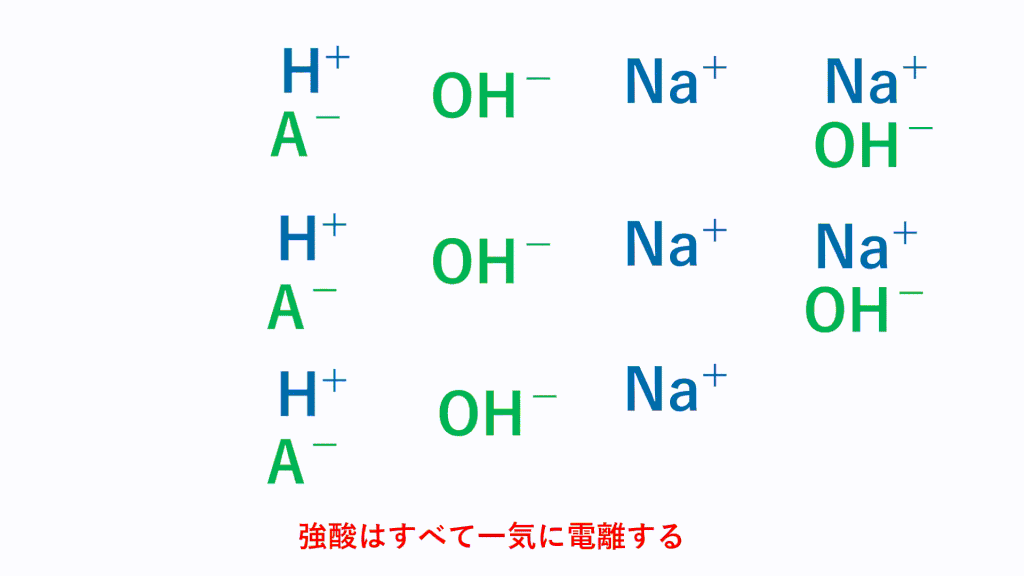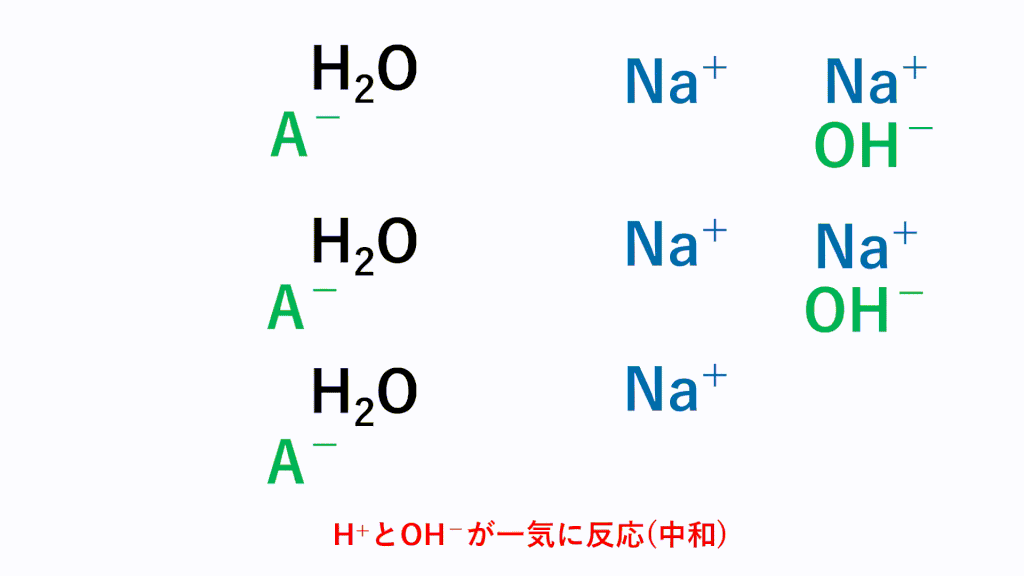
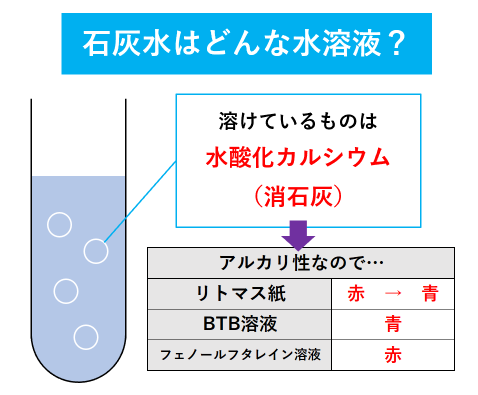
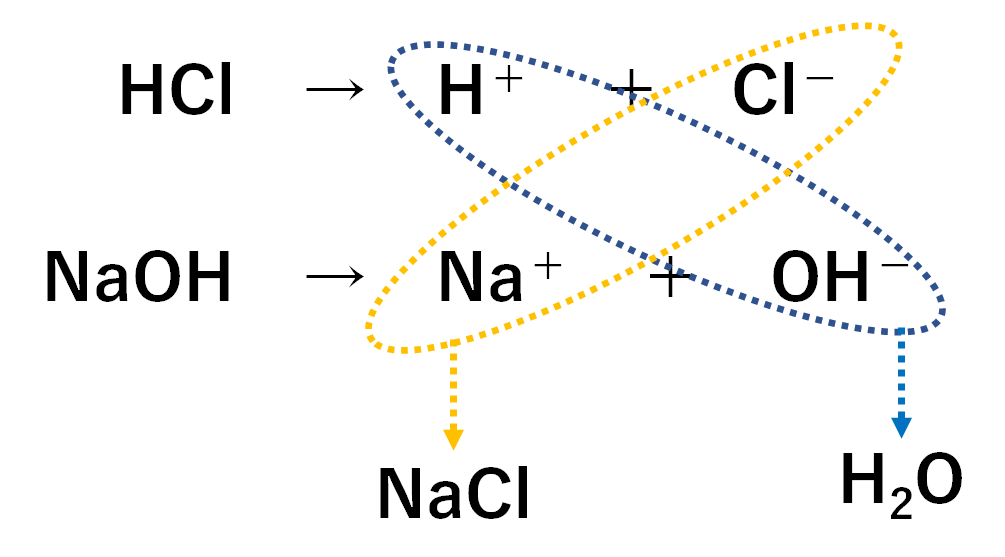
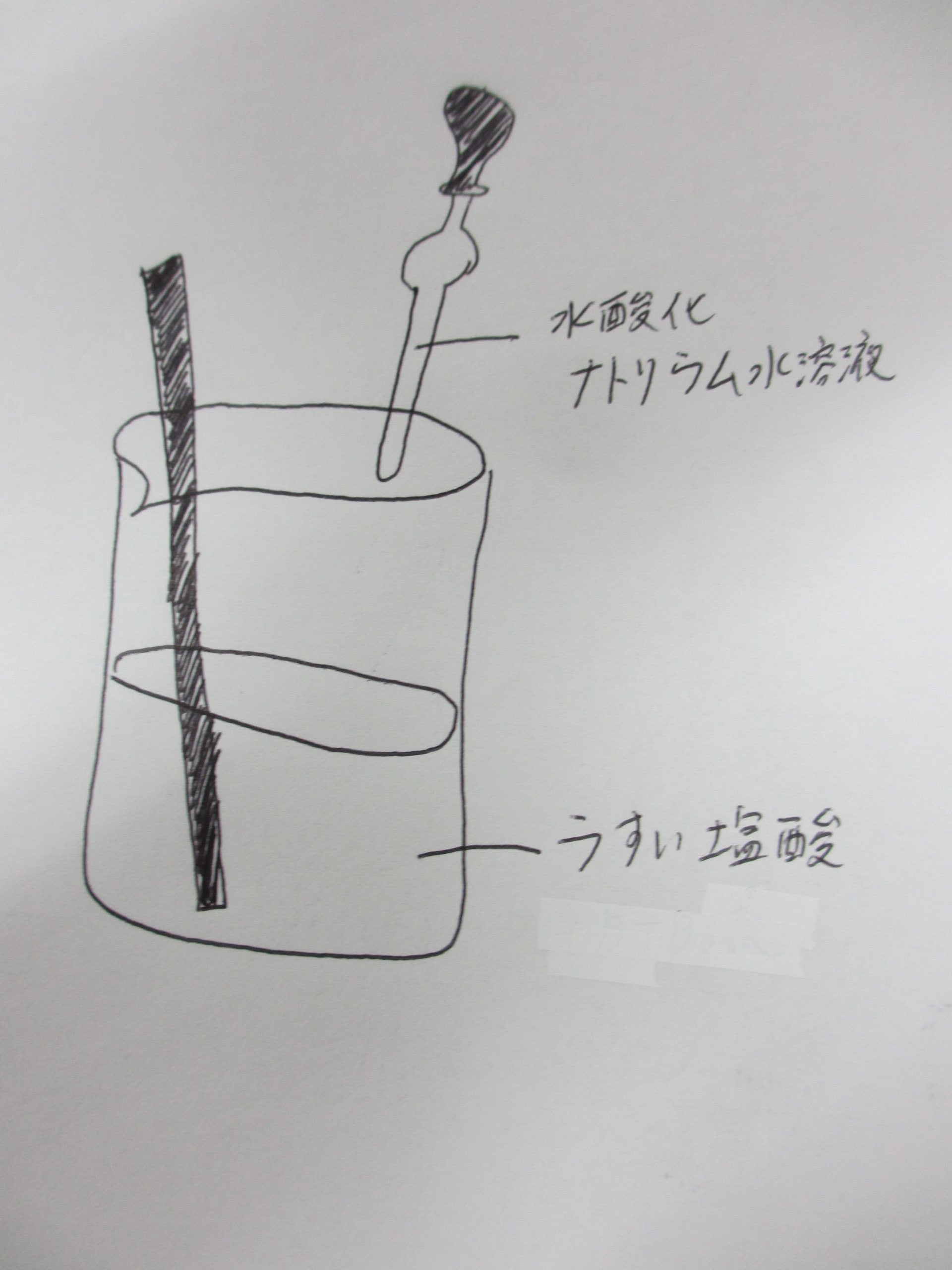
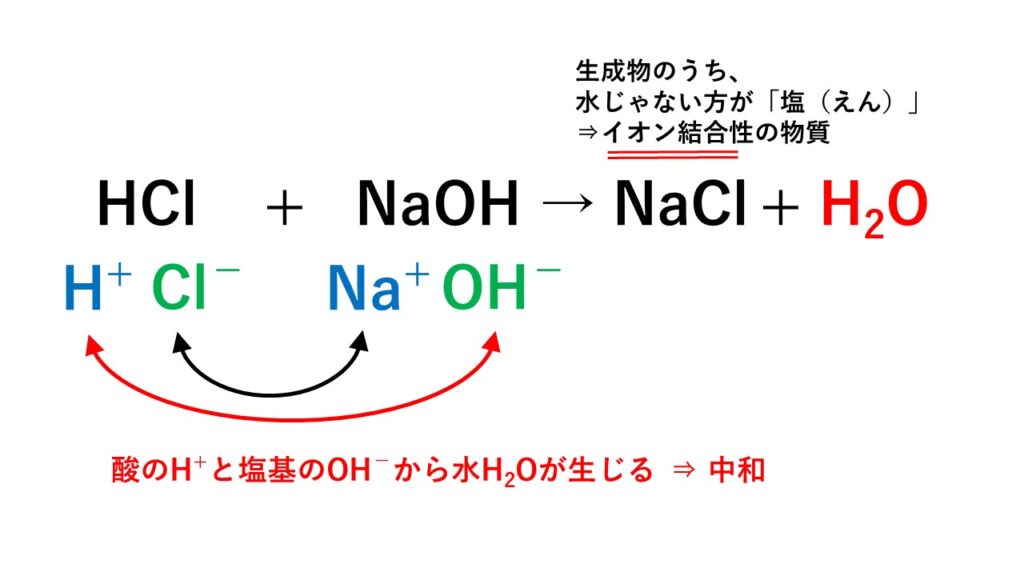
塩酸と水酸化ナトリウム水溶液の反応 HCl NaOH → NaCl H 2 O 酸性である塩酸の水素イオンと、アルカリ性である水酸化ナトリウムの水酸化物イオンが結びついて、水になることで中和され ベストアンサー まおゆうの虫 さん 6 07 お答えさせて頂きます。 鉄、マグネシウム など大抵の金属はアルカリ性の水溶液には解けません。 金属が水溶液に溶けると自ら 水酸化カルシウム アルカリ性 水酸化ナトリウム水溶液 水酸化ナトリウム アルカリ性 溶質の名前がそのまま使われている水溶液が多いですね。 ただし、食塩をとかした場合には塩化
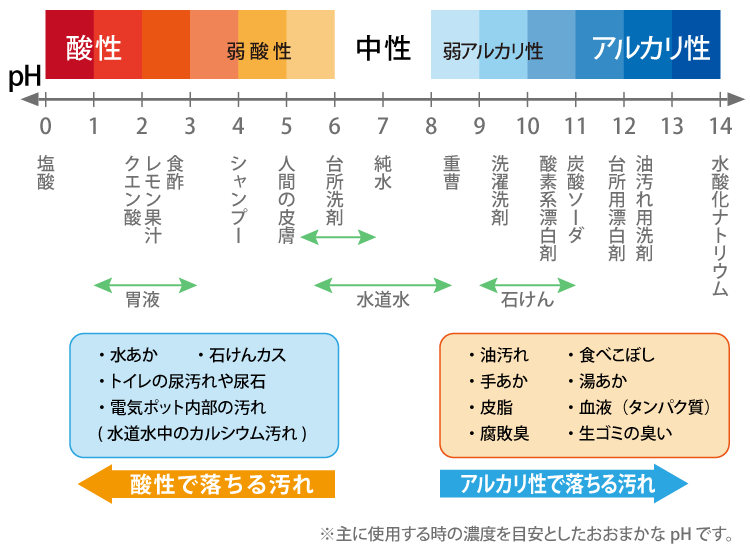
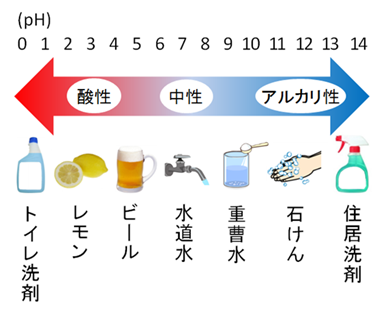
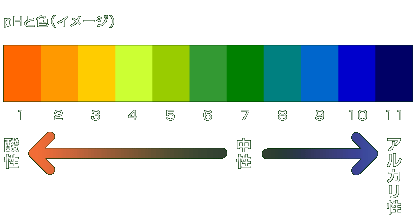
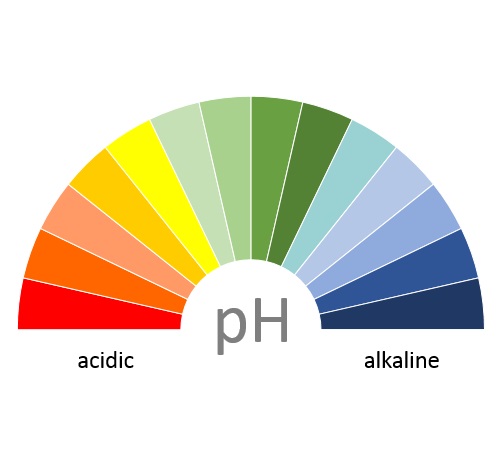
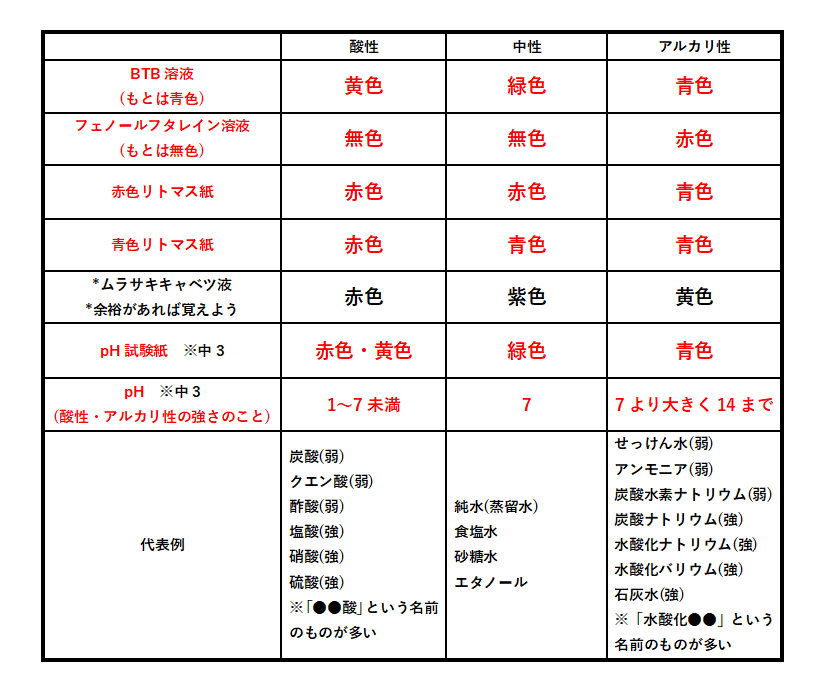
化学吸収法とは、「吸収塔」でアミン等のアルカリ性水溶液 (吸収液)とCO 2 含有ガスとを接触させ、吸収液にCO 2 を選択的に吸収させた後、「再生塔」で吸収液を加熱して、高純度のCO 2 を分酸性とアルカリ性の水溶液 フォローする 運営者情報;ホーム 理科解説 中3 化学変化とイオン 酸性とアルカリ性の水溶液 中3 化学 イオンの表し方とイオン式
アルカリ性 水溶液 化学式のギャラリー
各画像をクリックすると、ダウンロードまたは拡大表示できます
 |  | |
 |  | |
 |  | |
「アルカリ性 水溶液 化学式」の画像ギャラリー、詳細は各画像をクリックしてください。
 | ||
 |  |  |
 |  |  |
「アルカリ性 水溶液 化学式」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 |  |  |
 |  |  |
「アルカリ性 水溶液 化学式」の画像ギャラリー、詳細は各画像をクリックしてください。
 | ||
 |  |  |
 |  | |
「アルカリ性 水溶液 化学式」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 |  |  |
 |  | |
「アルカリ性 水溶液 化学式」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 |  | |
 |  | |
「アルカリ性 水溶液 化学式」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 |  | |
 |  |  |
「アルカリ性 水溶液 化学式」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |  |  |
 |  | |
「アルカリ性 水溶液 化学式」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |  |  |
 |  |  |
「アルカリ性 水溶液 化学式」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 |  |  |
 |  |  |
「アルカリ性 水溶液 化学式」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |  |  |
 |  | |
「アルカリ性 水溶液 化学式」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |
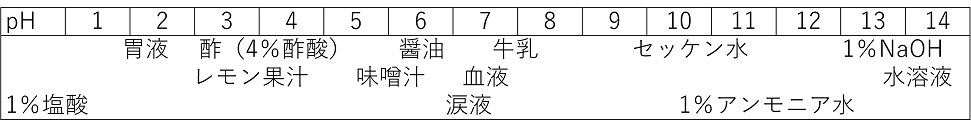
水溶液は、水(H 2 O)が溶媒である任意の 溶液です。 化学反応式では、記号(aq)が種名の後に続き、水溶液中であることを示します。たとえば、塩を水に溶かすと化学反応が起こります。 (1) 水溶性の性質 水溶液は、その性質によって、 酸性 、 中性 、 アルカリ性 に分けられます。 (2) 酸性 酸性の水溶液には、次のような特徴があります。 ?
Incoming Term: アルカリ性 水溶液 化学式,




0 件のコメント:
コメントを投稿